|
Tratamiento
Inicialmente es recomendable el reposo, pero se debe
programar un régimen de ejercicios de forma precoz, que
comience 2-3 semanas después del tratamiento
farmacológico.
El
primer fármaco a emplear es la prednisona (1 mg/Kg/d),
inicialmente en dosis divididas y posteriormente en
dosis única matutina. Se suelen requerir varias semanas
para que se produzca una mejoría clínica, a partir de
las cuales se comienza la reducción progresiva de la
dosis, hasta llegar aproximadamente a los 5-10 mg/d. En
casos graves, se pueden administrar inicialmente pulsos
de metilprednisolona (500-1000 mg/d durante 3 días)
seguidos de prednisona a las dosis ya indicadas, con la
finalidad de controlar mas rápidamente la inflamación.
Es
recomendable efectuar una prueba de la tuberculina, por
la posibilidad de que se reactive una tuberculosis con
el tratamiento esteroideo. También se debe disponer de
una densitometría ósea basal y prescribir calcio,
vitamina D y, eventualmente bifosfonatos, como
profilaxis de osteoporosis corticoidea.
Se
debe considerar siempre la adición de otros agentes a la
prednisona, como el metotrexato (7,5 a 25 mg semanales)
o la azatioprina (50 mg, 2 o 3 veces al día). Esta
combinación terapéutica está especialmente indicada en
las siguientes circunstancias: 1) necesidad de “ahorrar”
corticoides, para evitar sus efectos secundarios (p.ej.
pacientes diabéticos); 2) imposibilidad de reducir dosis
altas de corticoides por la aparición de una
exacerbación; 3) respuesta parcial a dosis altas de
corticoides después de 2 meses de tratamiento; y 4)
debilidad muscular rápidamente progresiva con
insuficiencia respiratoria.
El
metotrexato actúa más rápidamente que la azatioprina,
que puede requerir varios meses para alcanzar su efecto
máximo. Puesto que rara vez el metotrexato produce
toxicidad pulmonar, se debe evaluar la función pulmonar
antes de iniciar dicho tratamiento para excluir la
posibilidad de una enfermedad pulmonar intersticial
asociada a la MII.
En los
pacientes que no responden a la combinación de
corticoides y metotrexato se puede añadir azatioprina,
aunque se han descrito crisis febriles agudas con la
combinación de estos dos inmunosupresores. Otros agentes
que se reservan para los fracasos terapéuticos son (Fig.
1): inmunoglobulinas intravenosas -IGIV- (2 g/Kg a
intervalos mensuales durante 6 meses y posteriormente
cada 6-8 semanas), ciclosporina A (2,5-4 mg/Kg/d) y
micofenolato mofetilo (1 g, 2 o 3 veces al día). No
obstante, se debe considerar que un sujeto de más de 50
años con una supuesta PM que no responde al tratamiento
tiene una MCI mientras no se demuestre lo contrario.
Fig. 1: Esquema de tratamiento en la polimiositis y
dermatomiositis
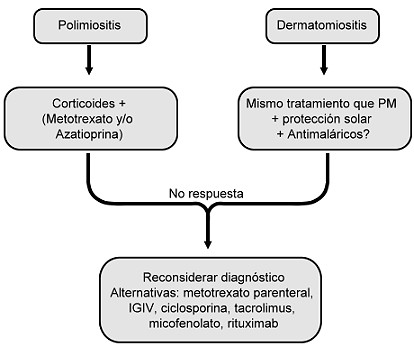
IGIV,
inmunoglobulinas intravenosas
Las
manifestaciones cutáneas de la DM pueden evolucionar de
forma independiente de las musculares. Dado que las
lesiones son fotosensibles, se recomendará protección
solar y uso de cremas con factor de protección superior
a 15. La hidroxicloroquina es efectiva en la mayoría de
los pacientes para controlar las lesiones cutáneas. Es
posible que los pacientes con DM tengan un mayor riesgo
de desarrollar erupciones morbiliformes con la
hidroxicloroquina. También parecen eficaces para mejorar
o resolver la enfermedad cutánea el metotrexato, las
IGIV y el micofenolato. El uso de tacrolimus tópico
(0,03-0,1%) puede resultar útil en erupciones
resistentes a otros tratamientos e incluso puede
aplicarse en la cara, aunque en ocasiones provoca
sensación de quemazón y prurito. La calcinosis es
especialmente difícil de tratar y aunque se pueden
probar diversos agentes (colchicina, diltiacem,
warfarina, corticoides) ninguno ha demostrado un
beneficio consistente. En ocasiones, es necesaria la
extirpación quirúrgica de las calcificaciones.
Durante el seguimiento del paciente, la medición de la
fuerza muscular y la determinación seriada de enzimas
musculares (p.ej. cada 2-3 meses) es útil, si bien las
modificaciones terapéuticas deben basarse en la
sintomatología clínica y no en las alteraciones
serológicas. Una complicación del uso de corticoides que
tiene especial relevancia en los pacientes con MII es la
miopatía esteroidea, ya que en ambas situaciones se
produce debilidad muscular proximal. La existencia de
enfermedad activa extramuscular (p.ej. piel, pulmón)
junto con cifras elevadas de CK indican una miositis
activa y hacen recomendable incrementar la dosis de
corticoides. Por el contrario, una debilidad progresiva
en el contexto de una dosis estable de corticoides sin
cambio en las enzimas musculares, sugiere toxicidad y,
en consecuencia favorece la reducción de la dosis del
fármaco. No obstante, en muchas ocasiones no hay más
remedio que aumentar o disminuir la dosis de corticoides
de forma empírica y evaluar el efecto clínico de esta
decisión.
En la
tabla 4 se resumen las principales características
clínicas diferenciales entre las tres formas de MII.
Tabla 4: Características diferenciales de las tres
formas principales de miopatía inflamatoria
|
Características |
Dermatomiositis |
Polimiositis |
Miositis con
cuerpos de inclusión |
|
Población afectada |
Niños y adultos (mujeres > varones) |
Adultos (mujeres > varones) |
Varones >50 a. |
|
Forma de instauración |
Subaguda (aguda) |
Subaguda |
Crónica |
|
Debilidad muscular |
Proximal |
Proximal |
Proximal y distal |
|
Lesión cutánea |
Sí (>90%) |
No |
No |
|
Neoplasias asociadas |
15-20% adultos |
+/- |
+/- |
|
Enzimas musculares (CK) |
Aumentadas |
Aumentadas |
Normales o ligero incremento |
|
Electromiograma |
Patrón miopático |
Patrón miopático |
Patrón miopático y neuropático |
|
Conectivopatías asociadas |
Esclerodermia, EMTC |
Sí, con todas |
Raro |
|
Respuesta al tratamiento |
++ |
+ |
Escasa |
|
Histología muscular:
Infiltrado celular
Depleción capilar
Depósito vascular de SC5b-9
Atrofia perifascicular
Invasión celular
parcial
Vacuolas ribeteadas |
B, CD4+
Sí
Sí
Sí
No
No |
CD8+
No
No
No
Sí
No |
CD8+
No
No
No
No
Sí |
CK,
creatincinasa; EMTC, enfermedad mixta del tejido
conectivo
|
|
|
|
|
|
|
|
|
|
|
Artículos
Especiales en
Clínica-UNR.org
de estos autores: |
|
|
|
|
|
|
|
|
|
|
|